Vers la localisation des dysfonctions rétiniennes
Achetée sur Istockphoto.com. Droit d’auteur.
L’électrorétinogramme est le seul outil objectif présentement accessible aux ophtalmologistes pour évaluer la fonction de la rétine. Malheureusement, cette réponse électrique nous donne seulement une idée globale de la fonction de la rétine, sans nous permettre de localiser précisément les possibles dommages fonctionnels. Nous présentons ici une nouvelle technique d’enregistrement qui permettrait de reconstruire la topographie de cette fonction et ainsi de localiser les possibles lésions ou dysfonction des cellules rétiniennes. Cette nouvelle technique d’imagerie permettrait de détecter et de faire un meilleur suivi de plusieurs maladies dégénératives rétiniennes. Mots clés Rétine, Reconstruction d’images, Problèmes inverses, Électrorétinogramme, Multiélectrodes, Électrodes virtuelles
L’utilité de l’électrorétinogramme
La première couche de cellule qui reçoit la lumière et la transmet ensuite au cerveau se nomme la rétine. Pour évaluer objectivement sa fonction, les cliniciens peuvent seulement compter sur l’électrorétinogramme (ERG), le signal électrique produit par celle-ci en réponse à un flash de lumière. Pour enregistrer l’ERG, une électrode active est placée sur l’œil ou autour de celui-ci, une électrode de référence est placée sur la tempe et une électrode de mise à la terre est placée sur le front [1]. Puis, le sujet est positionné devant un Ganzfeld, qui permet la stimulation de la rétine par un flash dans un environnement de lumière contrôlé. Malheureusement, comme ce test se fait avec seulement une électrode active et un flash qui illumine toute la rétine, la réponse enregistrée donne uniquement une idée globale de la fonction de la rétine. Il est donc impossible de déterminer l’endroit sur la rétine où il y aurait une possible dysfonction des cellules, ce qui limite le pouvoir diagnostique de cet outil clinique. Notre étude tente de remédier à cette lacune en augmentant le nombre d’électrodes pour pouvoir reconstruire la topographie de la fonction rétinienne.
Le principe de l’électrorétinogramme multiangulaire
Comme la surface de l’œil est petite, nous avons développé une nouvelle technique pour enregistrer l’ERG, qui multiplie virtuellement le nombre d’électrodes tout en limitant leur nombre total présent autour de l’œil, réduisant ainsi l’inconfort du sujet durant l’examen. Ceci est réalisable grâce aux rotations possibles de l’œil. Chaque angle du regard change= la position relative des quelques électrodes utilisées par rapport à la rétine. Ceci crée de multiples électrodes virtuelles qui enregistrent des réponses quasi simultanées, synchronisées par le flash de lumière. Puisque cette technique repose sur différents angles du regard, nous avons nommé cette technique l’ERG multiangulaire (ou maERG). Au total, seulement 3 électrodes réelles sont placées autour de l’œil. Avec les 11 positions du regard, nous obtenons 33 électrodes virtuelles, enregistrant 33 signaux ERG.
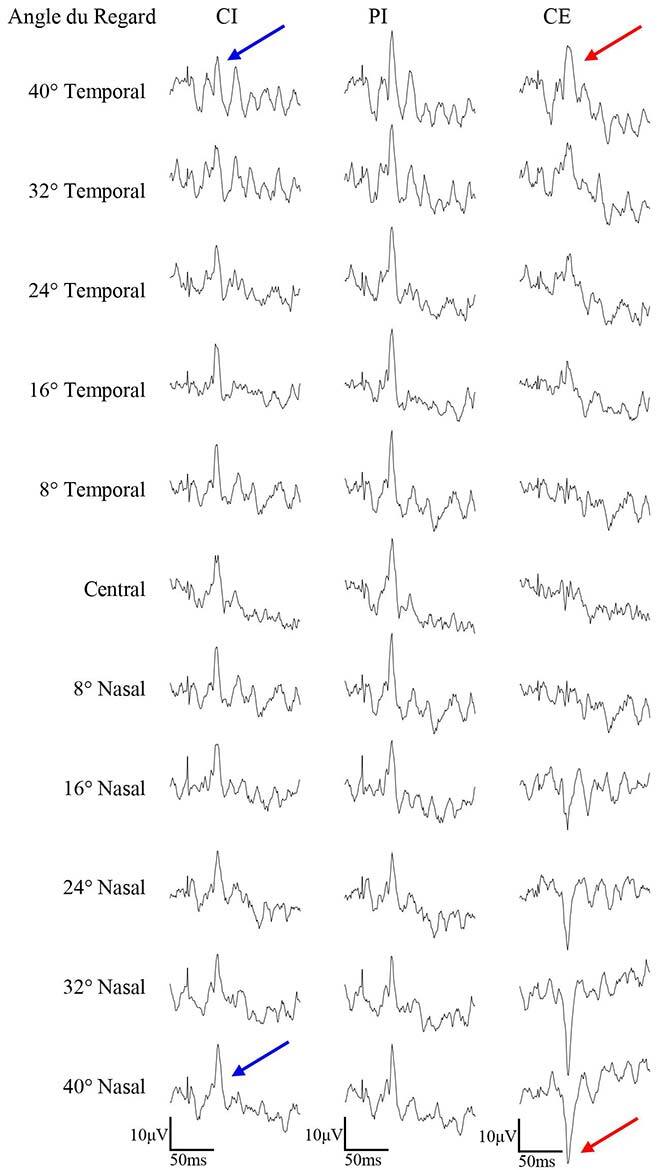
Fig. 1. Exemple d’enregistrements de 33 signaux du maERG chez un sujet normal. 11 positions du regard sont utilisées, de 40° Temporal à 40° Nasal (de gauche à droite), combinées à 3 électrodes réelles, placées sur le canthus interne (CI), la paupière inférieure (PI) et le canthus externe (CE). Les flèches blues et rouges montrent le changement de l’onde avec le changement du regard.
En combinant ces 33 signaux à un modèle électroanatomique de l’œil, nous pouvons calculer la topographie fonctionelle de l’activité rétinienne. Ceci équivaut à solutionner un problème inverse similaire à ce qui est fait en neuro-imagerie (en utilisant l’algorithme LORETA [2]). Ainsi, nous produisons la carte de l’activité bioélectrique de la rétine qui explique les enregistrements obtenus sur les électrodes virtuelles.
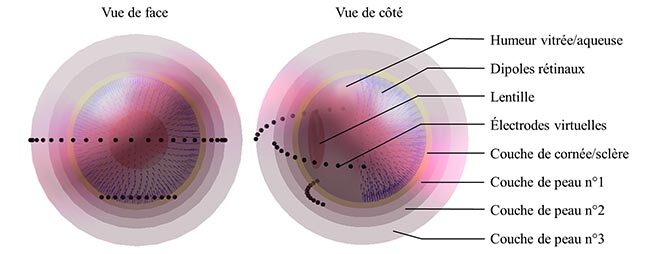
Fig. 2. Modèle électrophysiologique de l’œil, vu de face et de côté, avec les différents éléments le composant, indiqués à droite.
Simulations d’enregistrements et de reconstruction
Pour vérifier la faisabilité de notre technique de maERG, nous avons simulé des pathologies de la rétine, en faisant varier des zones inactives (ou scotomes) de tailles et de positions différentes. De plus, nous avons évalué la robustesse de l’algorithme de reconstruction en faisant varier le rapport signal-sur-bruit sur les mesures.
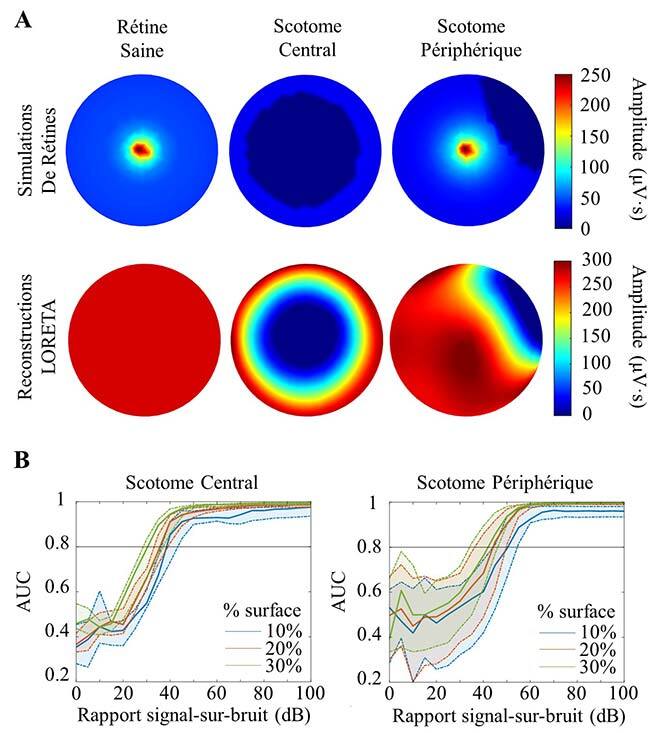
Fig. 3. (A) Représentation des différentes simulations des rétines avec l’image de leur reconstruction en dessous. (B) Aire sous la courbe (AUC; area under the curve) d’une courbe ROC (Receiver Operating Characteristic; courbe de sensibilité/spécificité) pour chaque simulation d’un différent rapport signal sur bruit, pour déterminer le niveau acceptable de bruit dans le modèle (dois dépasser un AUC de 0,8 pour être considéré comme valable).
Nos simulations ont démontré une variation de la qualité de la reconstruction en fonction de la localisation et de la taille du scotome, et l’influence d’un bon rapport signal sur bruit. En effet, si le scotome est central (c.-à-d., dans la région maculaire) et qu’il fait au moins 10 % de la surface de la rétine, il faut un rapport d’au moins 40 dB. Pour ce qui est des scotomes périphériques de même grandeur, un rapport d’au moins 55 dB est nécessaire pour obtenir une reconstruction valide. Il est donc plus facile de reconstruire l’activité au centre de la rétine que celle aux extrémités.
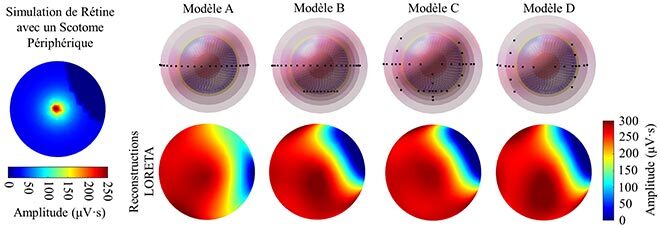
Fig. 4. Simulations de différents modèles de combinaisons d’électrodes ou de positions du regard. Modèle A : seulement 2 électrodes sur le même axe horizontal, avec 11 positions du regard horizontales. Modèle B : 3 électrodes, 2 sur le même axe horizontal et une plus bas verticalement, avec 11 positions du regard horizontales. Modèle C : 3 électrodes, 2 sur le même axe horizontal et une plus bas verticalement, avec 6 positions du regard horizontales et 5 verticales. Modèle D : seulement 2 électrodes sur le même axe horizontal, avec 6 positions du regard horizontales et 5 verticales. Seulement le modèle A ne réussit pas à reproduire l’activité rétinienne de la simulation.
Finalement, nous avons aussi vérifié quel étaient les positions d’électrodes virtuelles les plus utiles. L’idée de départ était d’utiliser 11 positions du regard sur le même axe horizontal (de gauche à droite), combiné à 3 électrodes, dont 2 sur le même axe horizontal et une placée plus bas, ce qui nous donne une autre information sur la verticale. Les résultats des différentes simulations étudiées nous ont démontré que l’important est d’avoir des électrodes sur tous les axes, que ce soit en plaçant une vraie électrode sur un autre axe (comme dans notre placement original) ou en déplaçant le regard aussi sur l’axe vertical (de haut en bas).
Conclusion
Cette étude présentait pour la première fois une technique non invasive d’enregistrement de l’ERG qui permette d’imager l’activité de la rétine sur 180°, afin de localiser les zones inactives ou dysfonctionnelles. Le maERG ouvre un nouveau champ de diagnostic et de suivi des patients qui sont atteints de maladies dégénératives en suivant l’évolution des régions atteintes aux fils des visites. Ceci est particulièrement important pour localiser les lésions qui commencent souvent en périphérie pour plusieurs maladies, telles que le glaucome, qui est la principale cause de cécité dans le monde.
Information supplémentaire
Pour plus d’information sur cette recherche, consulter l’article suivant : M. Gauthier, A. Brassard-Simard, M. Gauvin, P. Lachapelle and J. -M. Lina, « Multi-Angular Electroretinography (maERG): Topographic mapping of the retinal function combining real and virtual electrodes, » in IEEE Transactions on Biomedical Engineering, doi: 10.1109/TBME.2021.3075617.



